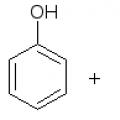
(skliausteliuose nurodyti koordinaciniai skaičiai) Ni 2+ 0,069 nm (4), 0,077 nm (5), 0,083 nm (6).
Vidutinis nikelio kiekis žemės plutoje yra 8-10 -3% masės, vandenynų vandenyje - 0,002 mg / l. Žinomas ca. 50 nikelio mineralų, iš kurių svarbiausi yra: pentlanditas (Fe, Ni) 9 S 8, milleritas NiS, garnieritas (Ni, Mg) 3 Si 4 O 10 (OH) 10. 4H 2 O, revdinskis (nepuitas) (Ni, Mg) 3 Si 2 O 5 (OH) 4, nikelis NiAs, annabergitas Ni 3 (AsO 4) 2 8H 2 O. Nikelis daugiausia kasamas iš sulfidinių vario-nikelio rūdų (Kanada, Australija, Pietų Afrika) ir iš silikatu oksiduotų rūdų (Naujoji Kaledonija, Kuba, Filipinai, Indonezija ir kt.). Apskaičiuota, kad pasaulio nikelio atsargos sausumoje siekia 70 mln.
Savybės. Nikelis-sidabras-baltas metalas. Kristalinis grotelės veido centre kub., a = 0,35238 nm, z = 4, tarpai. grupė Pt3t. T. pl. 1455 °C. t. kip. 2900 °С; plaustas. 8,90 g/cm3; C 0 p 26,l J / (mol. K); DH 0 pl 17,5 kJ / mol, DH 0 isp 370 kJ / mol; S 0 298 29,9 JDmol K); garų slėgio priklausomybės nuo temperatūros lygtis kietajam nikeliui lgp (hPa) \u003d 13,369-23013 / T + 0,520lgT + 0,395T (298-1728K), skystam lgp (hPa) \u003d T / 1042-8 +11,8. lg T (1728 m.3170 K); temperatūros koeficientas. tiesinis plėtimasis 13.5 . 10 -6 K -1 (273-373 K); šilumos laidumas 94,1 W / (m x x K), esant 273 K, 90,9 W / (m. K) esant 298 K; g 1,74 N/m (1520 °C); r 7,5 10 -8 omų m, temp. r 6,75. 10 -3 K -1 (298-398 K); feromagnetas, Curie taškas 631 K. Tamprumo modulis 196-210 GPa; s rast 280-720 MPa; susiję. pailgėjimas 40-50%; Brinelio kietumas (atkaitintas) 700-1000 MPa. Grynas nikelis yra labai lankstus metalas, gerai apdirbamas šaltoje ir karštoje būsenoje, tinka valcavimui, tempimui, kalimui.
H Nikelis yra chemiškai neaktyvus, tačiau smulkūs milteliai, gauti nikelio junginius redukuojant vandeniliu žemoje temperatūroje, yra piroforiniai. Standartinis elektrodo potencialas Ni 0 /Ni 2+ yra 0,23 V. Įprastoje temperatūroje ore esantis nikelis yra padengtas plona apsaugine nikelio oksido plėvele. Ne sąveika. su vandens ir oro drėgme. Kraunant nikelio oksidacija nuo paviršiaus prasideda ~ 800 °C temperatūroje. Nikelis labai lėtai reaguoja su druskos, sieros, fosforo, vandenilio fluorido rūgštimis. Praktiškai acto ir kitų org. jums, ypač kai nėra oro. Puikiai reaguoja su razb. HNO 3, koncentr. HNO 3 pasyvuotas. Šarminių ir šarminių metalų karbonatų tirpalai ir lydalai, taip pat skystas NH 3 neturi įtakos nikeliui. Vandens p-ry NH 3 dalyvaujant. oras koreliuoja nikelį.
H Išsklaidytas nikelis turi didelį katalizatorių. aktyvumas hidrinimo, dehidrogenavimo, oksidacijos, izomerizacijos, kondensacijos srityse. Naudojamas arba skeletinis nikelis (Raney nikelis), gaunamas legiruojant su Al arba Si su pastaruoju. išplovimas šarmu arba nikeliu ant nešiklio.
H Nikelis sugeria H 2 ir su juo sudaro kietus tirpalus. Hidridai NiH 2 (stabilūs žemesnėje nei 0 ° C temperatūroje) ir stabilesni NiH buvo gauti netiesiogiai. Nikelis azoto beveik nesugeria iki 1400 ° C, metalo N 2 p reikšmė 450 ° C temperatūroje yra 0,07%. Kompaktiškas nikelis nereaguoja su NH 3, dispersinis nikelis su juo sudaro Ni 3 N 300-450 ° C temperatūroje.
Išlydytas nikelis ištirpina C susidarant karbidui ir Ni 3 C, kuris suyra lydalo kristalizacijos metu, išsiskiriant grafitui; Ni 3 C pilkai juodų miltelių pavidalu (suyra ~ 450°C temperatūroje) gaunamas karburizuojant nikelį CO atmosferoje 250-400°C temperatūroje. Išsklaidytas nikelis su CO suteikia lakiojo nikelio tetrakarbonilo Ni(CO) 4 . Susiliejus su Si, susidaro s ir l bei c ir d s; Ni 5 Si 2 , Ni 2 Si ir NiSi lydosi tolygiai. esant 1282, 1318 ir 992 °C temperatūrai, Ni 3 Si ir NiSi 2 – atitinkamai nenuosekliai. 1165 ir 1125°C temperatūroje Ni 3 Si 2 suyra nesilydant 845°C temperatūroje. Susiliejus su B, susidaro boridai: Ni 3 B (temp. 1175 °C), Ni 2 B (1240 °C), Ni 3 B 2 (1163 °C), Ni 4 B 3 (1580 °С), NiB 12 (2320 °С), NiB (suyra esant 1600 °С). Su Se garais nikelis sudaro selenidus: NiSe (temp. 980 °C), Ni 3 Se 2 ir NiSe 2 (jie suyra atitinkamai 800 ir 850 °C temperatūroje), Ni 6 Se 5 ir Ni 21 Se 20 (egzistuoja tik kietoji būsena). Nikelį sulydžius su Te, gaunami teluridai: NiTe ir NiTe 2 (matyt, tarp jų susidaro įvairiausių kietų tirpalų) ir kt.
Arsenatas Ni 3 (AsO 4) 2. 8H 2 O-žalieji kristalai; tirpalas vandenyje 0,022%; to-tami suyra; virš 200 °С dehidratuoja, ~ 1000 °С temperatūroje suyra; kieto muilo katalizatorius.
Silicio dioksidas ir t Ni 2 SiO 4 – šviesiai žali kristalai su rombu. grotelės; tankus 4,85 g/cm3; suyra nelydant 1545°C temperatūroje; netirpsta vandenyje; kalnakasys. to-tami lėtai suyra kaitinant. Aliuminio oksidas t NiAl 2 O 4 (nikelio špinelis) - mėlyni kristalai su kub. grotelės; lyd.p. 2110°С; tankus 4,50 g/cm3; ne sol. vandenyje ; lėtai suyra iki tami; hidrinimo katalizatorius.
Svarbiausias kompleksas Kom. nikelio-a m m ir n s. Naib. būdingi atitinkamai heksaaminai ir akvatetraminai su katijonais. 2+ ir 2+ . Tai mėlyni arba violetiniai kristalai. in-va, dažniausiai sol. vandenyje, ryškiai mėlynos spalvos tirpaluose; verdant tirpalus ir veikiant to-t suyra; susidaro tirpaluose apdorojant nikelio ir kobalto rūdas amoniaku.
Ni(III) ir Ni(IV) kompleksuose koordinacija nikelio skaičius yra 6. Pavyzdžiai yra violetinis K 3 ir raudonas K 2, susidaręs F 2 veikiant NiCl 2 ir KCl mišinį; stiprūs oksidatoriai. Iš kitų tipų yra žinomos, pavyzdžiui, heteropolirūgščių druskos. (NH4)6H7. 5H 2 O, daug chelato Comm. Ni(II). Taip pat žiūrėkite nikelio organiniai junginiai.
Kvitas. Rūdas apdoroja piro- ir gidromstal-lurgich. būdu. Silikatu oksiduotoms rūdoms (netinkamos sodrinti) naudokite arba atkurkite. lydymas, kad būtų gautas feronikelis, kuris vėliau įpučiamas konverteryje, kad būtų gryninamas ir sodrinamas, arba lydomas iki matinio su sieros turinčiais priedais (FeS 2 arba CaSO 4). Gautas matinis pučiamas į konverterį, kad būtų pašalintas Fe, o po to susmulkinamas ir išdeginamas, iš susidariusio NiO jis bus redukuotas. metalo nikelis gaunamas lydant. Nikelio koncentratai, gauti sodrinant sulfidines rūdas, lydomi į matinius su paskutiniu. išvalymas keitiklyje. Iš vario-nikelio dėmės, po lėto aušinimo flotacijos būdu, išskiriamas Ni 3 S 2 koncentratas, kuris, kaip ir dėmės iš oksiduotų rūdų, sudeginamas ir redukuojamas.
Vienas iš oksiduotų rūdų hidroapdirbimo būdų yra rūdos redukcija generatoriaus dujomis arba H 2 ir N 2 mišiniu su pastarosiomis. NH 3 ir CO 2 išplovimo tirpalas su oro prapūtimu. Tirpalas išvalomas iš Co amonio sulfidu. Tirpalui skaidant distiliuojant NH 3, nusėda nikelio hidroksokarbonatas, kuris arba kalcinuojamas, ir redukuojamas iš susidariusio NiO. lydymosi gauti nikelį, arba iš naujo išspręsti. NH 3 tirpale ir distiliavus NH 3 iš masės redukuojant H 2, gaunamas nikelis. Dr. būdas - oksiduotos rūdos išplovimas sieros rūgštimi autoklave. Iš gauto tirpalo jį išvalius ir neutralizavus nikelis slėgiu nusodinamas vandenilio sulfidu, o gautas NiS koncentratas apdorojamas kaip matinis.
Hidroapdirbant sulfidinio nikelio medžiagas (koncentratus, mačius) redukuojama iki oksidacijos autoklave. išplovimas NH 3 tirpalais (esant mažam Co kiekiui) arba H 2 SO 4 . Iš amoniako tirpalų, atskyrus CuS, nikelis slėgiu nusodinamas vandeniliu. Norėdami atskirti Ni,Taip pat naudojamas Co ir Cu iš amoniako tirpalų ekstraktas. metodus, naudojant, visų pirma, kompleksonus sudarončius ekstraktorius.
Oksidacinis išplovimas autoklave sulfatiniams tirpalams gauti naudojamas tiek prisodrintoms medžiagoms (matėms), kai į tirpalą perkeliamas nikelis ir kiti metalai, tiek prastiems piročio Fe 7 S 8 koncentratams. Pastaruoju atveju oksiduotas preim. pirotitas, leidžiantis išskirti elementinį S ir sulfido koncentratą, kuris toliau lydomas į nikelio matinį.
Siūlome įsigyti nikelio NP2 lakštus palankiomis sąlygomis:
- Didelis asortimento ir dydžių pasirinkimas.
- Galimas papildomas metalo apdirbimas – pjovimas, lenkimas, cinkavimas, perforavimas
- Prekyba gabalais ir ruošiniais
- Prekės realizavimas tiek didmenine, tiek mažmenine prekyba.
- Kainos be tarpininkų komisinių.
- Įvairūs mokėjimo būdai ir sąlygos.
- Lanksti nuolaidų sistema didmeniniams ir nuolatiniams partneriams.
- Nemokamas profesionalus patarimas.
- Galimybė preliminariai surinkti užsakymą sandėlyje.
- Greiti pristatymo laikai. Mokamų prekių siuntimas per dieną Maskvoje.
- Pristatymas į Rusijos regionus per 2-3 dienas. Esant poreikiui savarankiškai apskaičiuosime ir užsakysime transporto įmonės paslaugas. Pristatymas į transporto įmonės terminalą nemokamas.
- Prekių pakavimas pagal kliento reikalavimus. Galima naudoti kelių tipų pakuotes: PET poliesterio apskritimą ir PVC polietileno plėvelę.
- Galimybė laikyti prekes mūsų sandėlyje iki išsiuntimo.
- Prekių grąžinimas pagal Rusijos Federacijos teisės aktus.
Asortimento charakteristikos ir dydžiai.
Nikelio lakštas NP2 yra plokščias stačiakampis pusgaminis, gaminamas karšto valcavimo būdu.
Nikelio lakšto pranašumai yra šie:
- didelio stiprumo;
- atsparumas korozijos sunaikinimui;
- atsparumas ekstremalioms temperatūroms;
- magnetinės savybės (feromagnetas).
Gaminio charakteristikas lemia nikelio markės NP2 savybės – vadinamasis. nikelio pusgaminiai pagal GOST 492-2006. Standartas reguliuoja priemaišų (anglies, vario, geležies, magnio ir kt.) kiekį metale – iš viso ne daugiau kaip 0,5 % masės. Medžiaga pasižymi atsparumu karščiui (atspari mechaniniam įtempimui aukštoje temperatūroje), atspari korozijai daugelyje agresyvių aplinkų, taip pat ir aukštesnėje temperatūroje (ši savybė apibrėžiama kaip atsparumas karščiui).
Lakšto storis pagal GOST svyruoja nuo 5 iki 20 mm, plotis - 500, 600, 700, 800 mm, ilgis 500-2000 mm. Galite nusipirkti lakštų iš nikelio matuoto ilgio, kartotinio 100 mm, ir atsitiktinių, visiškai atitinkančių valstybės standartus.
Gaminio kokybė kontroliuojama visuose gamybos proceso etapuose. Medžiagos paviršius atitinka standartus ir neturi delaminacijų, mechaninių pažeidimų ir kitų defektų.
GOST, TU ir kiti standartai.
Specifikacijų lapas NP2, nustatytas pagal GOST 6235-91. Aukštą gaminio gamybos ir apdailos tikslumą reglamentuoja GOST 26877-2008. Nikelio NP2 cheminė sudėtis atitinka GOST 492-2006.
Taikymo sritys.
Geros mechaninės, elektrinės, antikorozinės savybės paskatino plačiai naudoti NP2 lakštą. Visų pirma, jo naudojimas yra pateisinamas gamyboje, kur keliami aukšti reikalavimai medžiagos atsparumui korozijai. Pagrindinės naudojimo kryptys:
- laivų statyba;
- mechaninė inžinerija, instrumentų gamyba;
- elektros dalys - katodai, anodai;
- chemijos pramonei skirtų produktų gamyba – talpos, katilai, indai, kurie sąveikauja su agresyviomis medžiagomis.
Nikelio lakštų pardavimas iš sandėlio Maskvoje.
Nikelio lakštų pardavimas vykdomas iš sandėlio Maskvoje, esančio adresu:
111123, Maskva, sh. Entuziastovas, 56 m., 44 pastatas
Apmokėtas prekes galite gauti pristatymo būdu arba pristatymo būdu, kurį atliks mūsų įmonė. Mūsų nuosavas automobilių parkas, susidedantis iš įvairaus tonažo automobilių, leis nebrangiai ir operatyviai pristatyti užsakymą į Jūsų objektą.
Užsakant prekes nuo 100 kg. siuntimas jums bus nemokamas.
Sumokėtų prekių išsiuntimas ir pristatymas atliekamas per vieną dieną.
Nikelio sulfatas yra smaragdo žalios arba turkio spalvos kristalinė medžiaga, tirpstanti vandenyje, atšiauri ore. Tai viena iš nikelio druskų rūšių.
Nikelio sulfatas yra labai toksiška medžiaga, todėl dirbdami su juo turite laikytis pavojingų medžiagų tvarkymo taisyklių.
Cheminė formulė: NiSO4 7H2O.
Nikelio sulfatas naudojamas galvanizuojant gaminius ir metalus.
Taip pat - baterijų, katalizatorių, feritų gamybai elektronikos ir elektros pramonėje, metalurgijoje lydiniams ruošti. Nikelis plačiai naudojamas kvepalų, riebalų ir chemijos pramonėje kaip reagentas.
Keramikos gamyboje nikelio sulfatas naudojamas kaip dažiklis.
Nikelio sulfato (nikelio sulfato heptahidrato, nikelio vitriolio) saugos reikalavimai GOST 4465-74.
7-vandeninis nikelio sulfatas (II) yra kristalinė medžiaga. Prarijus, jis sukelia kancerogeninį ir bendrą toksinį poveikį. Patekus ant odos ir viršutinių kvėpavimo takų bei akių gleivinių, produktas dirgina ir sukelia padidėjusį jautrumą nikeliui.
Tirpinant vandenyje 7-vandeninį nikelio sulfatą (II), susidaro hidroaerozolis, kuris pagal poveikio organizmui laipsnį priskiriamas I pavojingumo klasės medžiagoms.
Didžiausia leistina 7-vandens nikelio sulfato hidroaerozolio koncentracija, išreikšta nikeliu, darbo zonos ore yra 0,005 mg/m³.
Didžiausia leistina nikelio jonų koncentracija sanitarinių rezervuarų vandenyje yra 0,1 mg/dm³.
7 vandens nikelio sulfato neutralizavimas ir sunaikinimas netaikomas. Išsiliejęs produktas po sauso ir vėlesnio drėgno valymo pašalinamas nikelio sulfato gamybos ar vartojimo technologiniuose procesuose.
Nikelio sulfatas nesudaro nuodingų medžiagų ore ir nuotekose.
7 vandens sulfatinis nikelis (II) yra nedegus, atsparus ugniai ir sprogimui.
Visi dirbantys su nikelio sulfatu turi būti aprūpinti specialia apranga, specialia avalyne ir kitomis apsaugos priemonėmis. Norint apsaugoti kvėpavimo sistemą, reikia naudoti respiratorių ShB-1 „Petal“. Kad nepatektų ant rankų odos, rekomenduojama naudoti apsauginę pastą IER-2 ir lanolino-ricinos tepalą. Jei nikelio sulfato pateko į akis, plaukite jas dideliu kiekiu vandens.
Gamybinėse ir laboratorinėse patalpose, kuriose dirbama su 7-vandens nikelio sulfatu, turi būti įrengta tiekimo ir ištraukiamoji ventiliacija, įranga turi būti sandari.
APIBRĖŽIMAS
Nikelis yra dvidešimt aštuntas periodinės lentelės elementas. Pavadinimas – Ni iš lotyniško „niccolum“. Įsikūręs ketvirtajame periode, VIIIB grupė. Nurodo metalus. Branduolinis krūvis yra 28.
Kaip ir kobaltas, nikelis gamtoje daugiausia randamas junginių su arsenu arba siera pavidalu; tokie, pavyzdžiui, mineralai kupfernikelis NiAs, arseno-nikelio blizgesys NiAsS ir kt. Nikelis yra labiau paplitęs nei kobaltas [apie 0,01% (masės) žemės plutos].
Metalinis nikelis yra sidabrinės spalvos su gelsvu atspalviu (1 pav.), yra labai kietas, gerai poliruojasi, traukia magnetas. Jis pasižymi dideliu atsparumu korozijai – stabilus atmosferoje, vandenyje, šarmuose ir daugelyje rūgščių. Jis aktyviai tirpsta azoto rūgštyje. Nikelio cheminis atsparumas atsiranda dėl jo polinkio pasyvuoti – ant paviršiaus susidaro oksidinės plėvelės, kurios turi stiprų apsauginį poveikį.
Ryžiai. 1. Nikelis. Išvaizda.
Nikelio atominė ir molekulinė masė
APIBRĖŽIMAS
Santykinė medžiagos molekulinė masė (M r) yra skaičius, rodantis, kiek kartų tam tikros molekulės masė yra didesnė nei 1/12 anglies atomo masės, ir santykinė elemento atominė masė (A r)- kiek kartų vidutinė cheminio elemento atomų masė yra didesnė už 1/12 anglies atomo masės.
Kadangi nikelis egzistuoja laisvoje būsenoje monoatominių Ni molekulių pavidalu, jo atominės ir molekulinės masės reikšmės sutampa. Jie lygūs 58,6934.
Nikelio izotopai
Yra žinoma, kad nikelis gamtoje gali atsirasti penkių stabilių izotopų 58Ni, 60Ni, 61Ni, 62Ni ir 64Ni pavidalu. Jų masės skaičiai yra atitinkamai 58, 60, 61, 62 ir 64. Nikelio izotopo 58 Ni branduolyje yra dvidešimt aštuoni protonai ir trisdešimt neutronų, o likę izotopai nuo jo skiriasi tik neutronų skaičiumi.
Yra dirbtinių nestabilių nikelio izotopų, kurių masės skaičius yra nuo 48 iki 78, taip pat aštuonios metastabilios būsenos, tarp kurių 59 Ni izotopas, kurio pusinės eliminacijos laikas yra 76 tūkst. metų, yra ilgiausias.
nikelio jonai
Elektroninė formulė, rodanti nikelio elektronų pasiskirstymą orbitoje, yra tokia:
1s 2 2s 2 2p 6 3s 2 3p 6 3d 8 4s 2 .
Dėl cheminės sąveikos nikelis atiduoda valentinius elektronus, t.y. yra jų donoras ir virsta teigiamai įkrautu jonu:
Ni 0 -2e → Ni 2+;
Ni 0 -3e → Ni 3+.
Nikelio molekulė ir atomas
Laisvoje būsenoje nikelis egzistuoja monoatominių Ni molekulių pavidalu. Štai keletas savybių, apibūdinančių nikelio atomą ir molekulę:
Nikelio lydiniai
Didžioji nikelio dalis naudojama įvairiems lydiniams su geležimi, variu, cinku ir kitais metalais gaminti. Nikelio pridėjimas prie plieno padidina jo kietumą ir atsparumą korozijai.
Nikelio lydiniai gali būti skirstomi į karščiui atsparius (nimoninis, inkonelis, hastelas [daugiau nei 60% nikelio, 15-20% chromo ir kitų metalų]), magnetinius (permalloy) ir specialių savybių lydinius (monel metalas, nikelis, konstantanas). , invar, platina).
Problemų sprendimo pavyzdžiai
1 PAVYZDYS
| Užduotis | Parašykite reakcijų lygtis, kurios gali būti naudojamos atliekant šias transformacijas: NiCl 2 → Ni → NiSO 4 → Ni(NO 3) 2 → Ni(OH) 2 → NiCl 2. Nubraižykite reakcijų, vykstančių tirpaluose joninėmis ir sutrumpintomis joninėmis formomis, lygtis. |
| Atsakymas | Įdėjus nikelio (II) chlorido tirpalą, kuris yra aktyvesnis už metalinį nikelį, galima gauti nikelio laisvoje formoje (pakeitimo reakcija): NiCl 2 + Zn → Ni + ZnCl 2; Ni 2+ + Zn 0 → Ni 0 + Zn 2+ . Nikelis ištirpsta praskiestoje sieros rūgštyje ir susidaro nikelio (II) sulfatas: Ni + H 2 SO 4 (atskiesti) → NiSO 4 + H 2; Ni 0 + 2H + → Ni 2+ + H2. Nikelio (II) nitratas gali būti gaunamas mainų reakcijos būdu: NiSO 4 + Ba(NO 3) 2 → Ni(NO 3) 2 + BaSO 4 ↓; SO 4 2- + Ba 2+ → BaSO 4 ↓. Veikiant nikelio (II) nitratą su šarmu, galima gauti nikelio (II) hidroksidą: Ni(NO 3) 2 + 2NaOH → Ni(OH) 2 ↓+ 2NaNO 3 ; Ni 2+ + 2OH - \u003d Ni (OH) 2 ↓. Nikelio (II) chloridas iš nikelio (II) hidroksido gali būti gaunamas neutralizuojant druskos rūgštimi: Ni(OH)2 + 2HCl → NiCl2 + 2H2O; OH - + H + \u003d H 2 O. |
2 PAVYZDYS
| Užduotis | Kokios masės nikelio (II) chlorido galima gauti pakaitinus 17,7 g nikelio ir 12 litrų chloro (n.o.)? Kokio tūrio 0,06 M tirpalo galima paruošti iš šios druskos masės? |
| Sprendimas | Parašykime reakcijos lygtį: Ni + Cl 2 \u003d NiCl 2. Raskime nikelio (molinė masė - 59 g / mol) ir chloro, kurie sureagavo, molių skaičių, naudodami problemos sąlygoje nurodytus duomenis: n (Ni) = m (Ni) / M (Ni); n (Ni) \u003d 17,7 / 59 \u003d 0,3 mol. n (Cl 2) \u003d V (Cl 2) / V m; n (Cl 2) \u003d 12 / 22,4 \u003d 0,54 mol. Pagal uždavinio lygtį n (Ni): n (Cl 2) = 1:1. Tai reiškia, kad chloro perteklius ir visi tolesni skaičiavimai turėtų būti atliekami naudojant nikelį. Raskime medžiagos kiekį ir gauto nikelio (II) chlorido masę (molinė masė 130 g / mol): n (Ni): n (NiCl2) = 1:1; n (Ni) \u003d n (NiCl 2) \u003d 0,3 mol. m (NiCl 2) = n (NiCl 2) × M (NiCl 2); m (NiCl 2) \u003d 0,3 × 130 \u003d 39 g. Apskaičiuokite 0,06 M tirpalo tūrį, kurį galima gauti iš 39 g nikelio (II) chlorido: V (NiCl 2) \u003d n (NiCl 2) / c (NiCl 2); V (NiCl 2) \u003d 0,3 / 0,06 \u003d 0,5 l. |
| Atsakymas | Nikelio (II) chlorido masė – 39 g, 0,06 M tirpalo tūris – 0,5 l (500 ml). |
1 skyrius. Charakteristikos.
2 skyrius. Buvimas gamtoje.
3 skyrius. Kvitas.
4 skyrius. Paraiška.
- 1 poskyris. Lydiniai.
- 2 poskyris. Nikeliavimas.
5 skyrius. Monetų kaldinimas.
Ni- tai aštuntosios grupės šoninio pogrupio elementas, ketvirtasis periodinės D. I. Mendelejevo cheminių elementų sistemos periodas, kurio atominis skaičius yra 28.
Charakteristikos nikelio
Ni- jis yra sidabriškai baltas, nesutepa ore. Jis turi į veidą orientuotą kubinę grotelę su laikotarpį a = 0,35238 HM, erdvės grupė Fm3m. Gryna forma gali būti apdorojama slėgiu. Tai feromagnetas, kurio Curie taškas yra 358 C.
Savitoji elektrinė varža 0,0684 μ Ohm∙m.
Linijinio šiluminio plėtimosi koeficientas α=13,5∙10-6 K-1 esant 0 C
Tūrinio šiluminio plėtimosi koeficientas β=38-39∙10-6 K-1
Tamprumo modulis 196-210 GPa.
Nikelio atomų išorinė elektroninė konfigūracija yra 3d84s2. Stabiliausia nikelio oksidacijos būsena yra nikelis (II).
Ni sudaro junginius su oksidacijos laipsniais +2 ir +3. Tuo pačiu metu Ni, kurio oksidacijos būsena yra +3, yra tik sudėtingų druskų pavidalu. Nikelio +2 junginiams žinoma daug paprastų ir sudėtingų junginių. Nikelio oksidas Ni2O3 yra stiprus oksidatorius.

Ni pasižymi dideliu atsparumu korozijai – jis yra stabilus ore, vandenyje, šarmuose ir daugelyje rūgščių. Cheminis atsparumas atsiranda dėl jo polinkio pasyvuoti – ant jo paviršiaus susidaro tanki oksido plėvelė, kuri turi apsauginį poveikį. Ni aktyviai tirpsta azoto rūgštyje.
Su anglies monoksidu CO Ni lengvai sudaro lakų ir labai toksišką nikelio karbonitą (CO)4.
Smulkiai disperguoti nikelio milteliai yra piroforiniai (savaime užsidega ore).
Ni dega tik miltelių pavidalu. Jis sudaro du nikelio O ir Ni2O3 oksidus ir atitinkamai du nikelio (OH) 2 ir nikelio (OH) 3 hidroksidus. Svarbiausios tirpios nikelio druskos yra acetatas, chloridas, nitratas ir sulfatas.


Tirpalai dažniausiai būna žalios spalvos, o bevandenės druskos – geltonos arba rudai geltonos spalvos. Netirpios druskos apima oksalatą ir fosfatą (žalią), tris sulfidus:
nikelis (juodas)
Ni3S2 (gelsva bronza)
Ni3S4 (sidabro baltas).
Ni taip pat sudaro daugybę koordinacinių ir sudėtingų junginių.
Vandeniniuose nikelio(II) druskų tirpaluose yra heksaakvanikelio(II) jonų nikelio(H2O)62+. Kai į tirpalą, kuriame yra šių jonų, įpilama amoniako tirpalo, nusėda nikelio (II) hidroksidas, žalia želatinos medžiaga. Šios nuosėdos ištirpsta įpylus perteklinį amoniako kiekį, nes susidaro heksamminenikelio (II) nikelio (NH3)62+ jonai.
Ni sudaro kompleksus su tetraedrinėmis ir plokščiomis kvadratinėmis struktūromis. Pavyzdžiui, tetrachloronikelato (II) NiCl42– komplekso struktūra yra tetraedrinė, o nikelio (CN) 42– tetracianonikelato (II) komplekso struktūra yra plokščia kvadratinė.
Atliekant kokybinę ir kiekybinę analizę nikelio (II) jonams aptikti naudojamas šarminis butandiondioksimo tirpalas, taip pat žinomas kaip dimetilglioksimas. Kai jis sąveikauja su nikelio (II) jonais, susidaro raudonas koordinacinis junginys bis (butanedioksimato) Ni (II). Tai yra chelatas, o butandionedioksimato ligandas yra dvidantis.
Natūralų Ni sudaro 5 stabilūs izotopai: 58 nikelis, 60 nikelis, 61 nikelis, 62 nikelis yra gausiausias (natūralus gausumas 68,077%).
Buvimas gamtoje
Ni yra gana dažnas gamtoje – jo kiekis žemės plutoje yra apie 0,01 % (masės). Žemės plutoje jis randamas tik surištas, geležies meteorituose yra vietinio Ni (iki 8%). Jo kiekis ultrabazinėse uolienose yra maždaug 200 kartų didesnis nei rūgštinėse (1,2 kg/t ir 8 g/t). Ultramafinėse uolienose vyraujantis nikelio kiekis siejamas su olivinais, kuriuose yra 0,13–0,41 % nikelio. Jis taip pat pakeičia magnį izomorfiškai.
Nedidelė dalis nikelio yra sulfidų pavidalu. Ni pasižymi siderofilinėmis ir chalkofilinėmis savybėmis. Padidėjus sieros kiekiui magmoje, atsiranda nikelio sulfidai kartu su variu, kobaltu, geležies ir platinoidai. Hidroterminiame procese kartu su kobaltu, arsenu ir pilka o kartais su bismutu, uranu ir sidabru Ni sudaro didesnę koncentraciją kaip nikelio arsenidai ir sulfidai. Ni dažniausiai randama sulfido ir arseno turinčiose vario-nikelio rūdose.
Nikelis (raudonas nikelio piritas, kupfernikelis) nikelis As.

Chloantitas (baltasis nikelio piritas) (nikelis, Co, Fe)As2
Garnieritas (Mg, nikelis)6(Si4O11)(OH)6 su H2O ir kitais silikatais.

Magnetinis piritas (Fe, nikelis, Cu)S
Arseno-nikelio blizgesys (gersdorfitas) nikelis As S,
Pentlanditas (Fe, nikelis) 9S8
Daug žinoma apie nikelį organizmuose. Nustatyta, kad, pavyzdžiui, jo kiekis žmogaus kraujyje kinta su amžiumi, kad gyvūnų organizme padidėja nikelio kiekis, galiausiai, yra keletas augalų ir mikroorganizmų – nikelio „koncentratorių“, kuriuose yra tūkst. ir net šimtus tūkstančių kartų daugiau nikelio nei Aplinka.
Kvitas
Bendros nikelio atsargos rūdose 1998 m. pradžioje buvo vertinamos 135 mln. tonų, įskaitant patikimas - 49 mln. taip pat yra arseno, geležies Ir sieros; Pentlandito inkliuzų pasitaiko ir magminiame pirotite. Kitose rūdose, iš kurių taip pat kasamas nikelis, yra Co priemaišų, Cu, Fe ir Mg. Kartais Ni yra pagrindinė prekė procesas rafinavimas, bet dažniau gaunamas kaip šalutinis produktas produktas kitų metalų technologijose. Iš patikimų atsargų, remiantis įvairiais šaltiniais, nuo 40 iki 66% nikelio yra oksiduotose nikelio rūdose (ONR),
33% sulfido. 1997 m. nikelio, pagaminto perdirbant OHP, dalis sudarė apie 40% pasaulio produkcijos. Pramoninėmis sąlygomis OHP skirstomas į du tipus: magnio ir geležies.
Ugniai atsparios magnio rūdos, kaip taisyklė, yra elektra lydomos feronikeliui (5-50% nikelis + Co, priklausomai nuo žaliavos sudėties ir technologinių savybių).
Labiausiai geležies – lateritinės rūdos apdorojamos hidrometalurginiais metodais, naudojant amoniako-karbonato išplovimą arba sieros rūgšties išplovimą autoklave. Priklausomai nuo žaliavų sudėties ir taikomų technologinių schemų, šių technologijų galutiniai produktai yra: nikelio oksidas (76-90% nikelio), sukepinimas (89% nikelio), įvairios sudėties sulfidų koncentratai, taip pat metalinis Ni. elektrolitiniai, nikelio milteliai ir kobaltas.
Mažiau geležies – nontronitinės rūdos išsilydo į matines. Įmonėse, veikiančiose visą ciklą, tolesnio apdorojimo schema apima nikelio oksido pavertimą, skrudinimą, elektrinį lydymą metaliniam nikeliui gauti. Pakeliui išgaunamas kobaltas gaminamas metalo ir (arba) druskų pavidalu. Kitas nikelio šaltinis: Pietų Velso anglių pelenuose Didžiojoje Britanijoje – iki 78 kg nikelio tonoje. Padidėjęs nikelio kiekis kai kuriose angliose, naftoje, skalūnuose rodo nikelio koncentracijos galimybę iškastinėmis organinėmis medžiagomis. Šio reiškinio priežastys dar nėra išaiškintos.
„Ni ilgą laiką nebuvo galima gauti plastinės formos dėl to, kad jame visada yra nedidelė sieros priemaiša nikelio sulfido pavidalu, esanti plonais, trapiais sluoksniais ties ribomis. metalo. Pridėjus nedidelį kiekį magnio į išlydytą nikelį, siera paverčiama junginiu su magniu, kuris nusėda grūdelių pavidalu, nepažeisdamas plastiškumo. metalo».
Didžioji nikelio dalis gaunama iš garnierito ir magnetinių piritų.

Silikato rūda redukuojama anglies dulkėmis rotacinėse vamzdžių krosnyse iki geležies-nikelio granulių (5-8% nikelio), kurios vėliau išvalomos iš sieros, kalcinuojamos ir apdorojamos amoniako tirpalu. Tirpalą parūgštinus, iš jo elektrolitiniu būdu gaunamas metalas.
Karbonilo metodas (Mond metodas). Pirma, vario-nikelio matinis gaunamas iš sulfido rūdos, per kurią aukštu slėgiu perduodamas kobaltas. Susidaro lengvai lakus tetrakarbonilnikelis nikelis(CO)4, o ypač grynas metalas išskiriamas terminio skaidymo būdu.
Aliuminioterminis nikelio išgavimo iš oksidinės rūdos metodas: 3NiO + 2Al = 3Ni + Al2O.
Taikymas
Lydiniai
Ni yra daugumos superlydinių, aukštos temperatūros medžiagų, naudojamų aviacijos ir kosmoso pramonėje jėgainių dalims, pagrindas.
monel metalas (65-67% nikelio + 30-32% Cu+ 1% Mn), atsparus karščiui iki 500°C, labai atsparus korozijai;
balta (585 yra 58,5% auksas ir sidabro ir nikelio (arba paladžio) lydinys (ligatūra);

Nichromas, atsparus lydinys (60% nikelis + 40% Cr);
Permalloy (76% nikelio + 17% Fe + 5% Cu + 2% Cr), pasižymi dideliu magnetiniu jautrumu ir labai mažais histerezės nuostoliais;

Invaras (65% Fe + 35% nikelis), kaitinant beveik nepailgėja;

Be to, nikelio lydiniai apima nikelio ir chromo-nikelio plienus, nikelio sidabrą ir įvairius atsparumo lydinius, tokius kaip konstantanas, nikelis ir manganinas.
Nikelio vamzdžiai naudojami kondensatorių gamybai vandenilio gamyboje, šarmams siurbti chemijos pramonėje. Nikelio chemikalams atsparūs įrankiai plačiai naudojami medicinoje ir moksliniuose tyrimuose. Ni naudojamas radarui, televizoriui, nuotolinio valdymo pultui procesus branduolinėje technologijoje.
Iš gryno nikelio gaminami didelio atsparumo korozijai ir fizinių savybių pastovumo cheminiai indai, įvairūs aparatai, prietaisai, katilai, o iš nikelio medžiagų - rezervuarai ir rezervuarai maisto produktams, chemikalams, eteriniams aliejams laikyti, šarmams transportuoti, šarminėms medžiagoms lydyti. šarmų.
Gryno nikelio miltelių pagrindu gaminami porėti filtrai, skirti filtruoti dujas, kurą ir kitus chemijos pramonės gaminius. industrija. Ni milteliai taip pat naudojami nikelio lydinių gamyboje ir kaip rišiklis kietų ir itin kietų medžiagų gamyboje.
Biologinis nikelio vaidmuo reiškia mikroelementų, reikalingų normaliam gyvų organizmų vystymuisi, skaičių. Tačiau mažai žinoma apie jo vaidmenį gyvuose organizmuose. Yra žinoma, kad Ni dalyvauja gyvūnų ir augalų fermentinėse reakcijose. Gyvūnams jis kaupiasi keratinizuotuose audiniuose, ypač plunksnose. Padidėjęs nikelio kiekis dirvožemyje sukelia endemines ligas – augaluose atsiranda negražių formų, o gyvūnams – akių ligas, susijusias su nikelio kaupimu ragenoje. Toksiška dozė (žiurkėms) - 50 mg. Ypač kenksmingi yra lakieji nikelio junginiai, ypač jo tetrakarbonilnikelis(CO)4. Nikelio junginių MPC ore svyruoja nuo 0,0002 iki 0,001 mg/m3 (įvairiems junginiams).
Ni yra pagrindinė alergijos (kontaktinio dermatito) su oda besiliečiantiems metalams (papuošalai, laikrodžiai, džinsinio segtukai) priežastis.
Europos Sąjungoje nikelio kiekis gaminiuose, kurie liečiasi su žmogaus oda, yra ribotas.
Nikelio karbonitas Nikelis (CO) yra labai toksiškas. Didžiausia leistina jo garų koncentracija gamybinių patalpų ore – 0,0005 mg/m3.
XX amžiuje buvo nustatyta, kad kasoje yra labai daug nikelio. Vartojant po insulino, nikelis pailgina insulino veikimą ir taip padidina hipoglikeminį aktyvumą. Ni veikia fermentinius procesus, askorbo rūgšties oksidaciją, pagreitina sulfhidrilo grupių perėjimą į disulfidines. Ni gali slopinti adrenalino veikimą ir sumažinti kraujospūdį. Per didelis nikelio suvartojimas organizme sukelia vitiligo atsiradimą. Ni nusėda kasoje ir prieskydinėse liaukose.
nikeliavimas
Nikeliavimas yra nikelio dangos sukūrimas ant kito metalo paviršiaus, siekiant apsaugoti jį nuo korozijos. Jis atliekamas galvaniniu būdu, naudojant elektrolitus, kuriuose yra nikelio(II) sulfato, natrio chlorido, boro hidroksido, paviršinio aktyvumo ir blizgiųjų medžiagų bei tirpių nikelio anodų. Susidariusio nikelio sluoksnio storis yra 12–36 µm. Paviršiaus blizgesio stabilumą galima užtikrinti vėliau chromuojant (chromo sluoksnio storis 0,3 µm).
Nikeliavimas be srovės atliekamas nikelio(II) chlorido mišinio ir natrio hipofosfito mišinio tirpale, esant natrio citratui:
NiCl2 + NaH2PO2 + H2O = nikelis + NaH2PO3 + 2HCl
procesas atliekamas esant pH 4–6 ir 95 °C temperatūrai
Labiausiai paplitęs yra elektrolitinis ir cheminis nikeliavimas. Dažniau nikeliavimas (vadinamasis matinis) gaminamas elektrolitiniu būdu. Labiausiai ištirta ir stabiliausia dirbti sulfatiniai elektrolitai. Pridėjus į elektrolitą, formuotojų blizgesį užtikrina vadinamasis šviesus nikeliavimas. Elektrolitinės dangos turi tam tikrą poringumą, kuris priklauso nuo pagrindo paviršiaus paruošimo kruopštumo ir nuo dangos storio. Norint apsisaugoti nuo korozijos, būtinas visiškas porų nebuvimas, todėl padengiama daugiasluoksnė danga, kuri vienodo storio yra patikimesnė nei vieno sluoksnio (pavyzdžiui, plieno). prekybos prekė dažnai padengiamas pagal schemą Cu – Nikelis – Cr).

Elektrolitinio nikeliavimo trūkumai yra netolygus nikelio nusėdimas ant reljefo paviršiaus ir neįmanoma padengti siaurų ir gilių skylių, ertmių ir kt. Cheminis nikeliavimas yra šiek tiek brangesnis nei elektrolitinis nikeliavimas, tačiau jis suteikia galimybę padengti vienodo storio ir kokybės dangą ant bet kurių reljefinio paviršiaus dalių, jei tik joms yra prieinamas sprendimas. Procesas pagrįstas nikelio jonų redukcijos reakcija iš jo druskų naudojant hipofosfitinį natrio mišinį (ar kitus redukuojančius agentus) vandeniniuose tirpaluose.
Nikeliavimas naudojamas, pavyzdžiui, dengiant cheminės įrangos dalis, automobilius, dviračius, medicinos instrumentus, prietaisus.
Ni taip pat naudojamas muzikos instrumentų stygoms vynioti.

monetų kaldinimas
Ni yra plačiai naudojamas monetų gamyboje daugelyje šalių. Jungtinėse Amerikos Valstijose 5 centų moneta šnekamojoje kalboje vadinama „Ni“.
Ni buvo monetų sudedamoji dalis nuo XIX amžiaus vidurio. Jungtinėse Valstijose terminas „Ni“ arba „Nikas“ iš pradžių buvo vartojamas vario-nikelio monetoms (skraidančiam ereliui), kurios 1857–1858 m. pakeitė vario nikelio 12% nikelio.

Dar vėliau, 1865 m., terminas, priskirtas trijų procentų nikelio kiekiui, padidėjo 25%. 1866 metais penki proc nikelis (25% nikelio, 75% vario). Kartu su proporcingu lydiniu šis terminas šiuo metu buvo vartojamas JAV. Beveik gryno nikelio monetos pirmą kartą buvo panaudotos 1881 m. Šveicarijoje, o ypač daugiau nei 99,9 % Ni iš penkių centų monetų buvo nukaldinta Kanadoje (tuo metu didžiausia nikelio gamintoja pasaulyje).
centai pagaminti iš nikelio" height="431" src="/pictures/investments/img778307_14_Britanskie_monetyi_v_5_i_10_penny_sdelannye_iz_nikelya.jpg" title="(!LANG:14. Didžiosios Britanijos 5 ir 10 centų" width="682" />!}
Italija 1909" height="336" src="/pictures/investments/img778308_15_Monetyi_iz_nikelya_Italiya_1909_god.jpg" title="(!LANG:15. Nikelio monetos, Italija 1909 m." width="674" />!}
Šaltiniai
Vikipedija – nemokama enciklopedija, Vikipedija
hyperon-perm.ru – Hyperon gamyba
cniga.com.ua – knygų portalas
chem100.ru – Chemiko vadovas
bse.sci-lib.com – žodžių reikšmė Didžiojoje sovietinėje enciklopedijoje
chemistry.narod.ru – chemijos pasaulis
dic.academic.ru – Žodynai ir enciklopedijos
Investuotojo enciklopedija. 2013 .
Sinonimai:- Nikaragva
Pažiūrėkite, kas yra „nikelis“ kituose žodynuose:
NIKELIS- (simbolis Ni), metalas, kurio atominė masė 58,69, serijos numeris 28, kartu su kobaltu ir geležimi priklauso Mendelejevo periodinės sistemos VIII grupei ir 4 eilutei. Oud. in. 8,8, lydymosi temperatūra 1452°. Savo įprastuose ryšiuose N. ... ... Didžioji medicinos enciklopedija
NIKELIS- (simbolis Ni), sidabriškai baltas metalas, PEREINAMASIS ELEMENTAS, atrastas 1751 m. Pagrindinės jo rūdos: sulfido nikelio-geležies rūdos (pentlanditas) ir nikelio arsenidas (nikelis). Nikelis turi sudėtingą valymo procesą, įskaitant diferencijuotą skilimą ... Mokslinis ir techninis enciklopedinis žodynas
NIKELIS- (vokiškas nikelis). Metalas yra sidabriškai baltos spalvos ir nėra grynos formos. Pastaruoju metu jis buvo naudojamas indams ir virtuvės reikmenims ruošti. Užsienio žodžių žodynas, įtrauktas į rusų kalbą. Chudinovas A.N., 1910. NIKELIS Vok. Nikelis… Rusų kalbos svetimžodžių žodynas
Nikelis- yra gana kietas pilkšvai baltas metalas, kurio lydymosi temperatūra yra 1453 laipsniai. C. Tai feromagnetinis, lankstus, plastiškas, stiprus ir atsparus korozijai bei oksidacijai. Nikelis dažniausiai yra...... Oficiali terminija
nikelio- aš, m. nikelio m. , vokiškai Nikelis. 1. Sidabriškai baltas ugniai atsparus metalas. BAS 1. Nikelis, žalingas sidabro rūdos kompanionas, gavo savo pavadinimą iš piktojo nykštuko, tariamai gyvenusio Saksonijos kasyklose, vardo. Fersmanas Zanimas. geochemija. 2. Viršutinis sluoksnis ... ... Istorinis rusų kalbos galicizmų žodynas
NIKELIS- (lot. Niccolum) Ni, periodinės sistemos VIII grupės cheminis elementas, atominis skaičius 28, atominė masė 58,69. Pavadinimas kilęs iš vokiško nikelio – piktosios dvasios, kuri tariamai trukdė kalnakasiams, pavadinimo. Sidabriškai baltas metalas; tankis 8,90 g/cm³, mp 1455… Didysis enciklopedinis žodynas
NIKELIS- NIKELIS, nikelis, vyras. (vokiškas nikelis). Sidabriškai baltas ugniai atsparus metalas, aukšt. įrankių, indų ir kt. gamybai. (Pagal kalnų dievybės vardą skandinavų mitologijoje.) Aiškinamasis Ušakovo žodynas. D.N. Ušakovas. 1935 1940... Ušakovo aiškinamasis žodynas