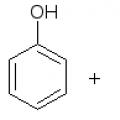
(bilangan koordinasi ditunjukkan dalam tanda kurung) Ni 2+ 0,069 nm (4), 0,077 nm (5), 0,083 nm (6).
Kandungan rata-rata nikel di kerak bumi adalah 8-10 -3% berat, di air lautan 0,002 mg / l. Dikenal sekitar 50 mineral nikel, di antaranya yang paling penting adalah: pentlandit (Fe, Ni) 9 S 8, millerit NiS, garnierit (Ni, Mg) 3 Si 4 O 10 (OH) 10. 4H 2 O, revdinskite (non-puit) (Ni, Mg) 3 Si 2 O 5 (OH) 4, nikel NiAs, annabergite Ni 3 (AsO 4) 2 8H 2 O. Nikel terutama ditambang dari bijih tembaga-nikel sulfida (Kanada, Australia, Afrika Selatan) dan dari bijih teroksidasi silikat (Kaledonia Baru, Kuba, Filipina, Indonesia, dll.). Cadangan nikel dunia di darat diperkirakan mencapai 70 juta ton.
Properti. Logam nikel-perak-putih. kristal kisi wajah terpusat kubik, a = 0,35238 nm, z = 4, spasi. kelompok Pt3t. T. pl. 1455 °C. t.kip. 2900 °С; rakit. 8,90 g/cm 3 ; C 0 p 26,l J / (mol. K); DH 0 pl 17,5 kJ / mol, DH 0 isp 370 kJ / mol; S 0 298 29,9 JDmol K); persamaan untuk ketergantungan suhu tekanan uap untuk lgp nikel padat (hPa) \u003d 13.369-23013 / T + 0.520lgT + 0,395T (298-1728K), untuk lgp cair (hPa) \u003d 11.742-20830/T + 0.618 lg T (1728-3170 K); koefisien suhu. ekspansi linier 13.5 . 10 -6 K -1 (273-373 K); konduktivitas termal 94,1 W / (m x x K) pada 273 K, 90,9 W / (m. K) pada 298 K; g 1,74 N/m (1520 °C); r 7,5 10 -8 ohm m, suhu. r 6.75. 10 -3 K -1 (298-398 K); ferromagnet, titik Curie 631 K. Modulus elastisitas 196-210 GPa; s rast 280-720 MPa; berhubungan. perpanjangan 40-50%; Kekerasan Brinell (anil) 700-1000 MPa. Nikel murni adalah logam yang sangat ulet, diproses dengan baik dalam keadaan dingin dan panas, cocok untuk digulung, ditarik, ditempa.
H Nikel secara kimia tidak aktif, tetapi bubuk halus yang diperoleh dengan mereduksi senyawa nikel dengan hidrogen pada suhu rendah bersifat piroforik. Potensial elektroda standar Ni 0 /Ni 2+ adalah 0,23 V. Pada suhu biasa, nikel di udara ditutupi dengan lapisan pelindung tipis oksida nikel. Bukan interaksi. dengan air dan kelembaban udara. Saat memuat oksidasi nikel dari permukaan dimulai pada ~ 800 °C. Nikel bereaksi sangat lambat dengan asam klorida, sulfat, fosfat, fluorida. Praktis, asetat dan org lainnya. untuk-Anda, terutama dengan tidak adanya udara. Merespon dengan baik dengan razb. HNO3 , kon. HNO3 dipasifkan. Solusi dan lelehan alkali dan karbonat logam alkali, serta NH 3 cair, tidak mempengaruhi nikel. Air p-ry NH 3 di hadapan. nikel berkorelasi udara.
H Nikel dalam keadaan terdispersi memiliki katalitik yang besar. aktivitas di distrik hidrogenasi, dehidrogenasi, oksidasi, isomerisasi, kondensasi. Baik nikel kerangka (nikel Raney) digunakan, diperoleh dengan paduan dengan Al atau Si dengan yang terakhir. pencucian dengan alkali, atau nikel pada pembawa.
H Nikel menyerap H2 dan membentuk larutan padat dengannya. Hidrida NiH2 (stabil di bawah 0 °C) dan NiH yang lebih stabil diperoleh secara tidak langsung. Nitrogen hampir tidak diserap oleh nikel hingga 1400 ° C, nilai p N 2 dalam logam adalah 0,07% pada 450 ° C. Nikel kompak tidak bereaksi dengan NH 3, nikel terdispersi membentuk Ni 3 N dengannya pada 300-450 ° C.
Nikel cair melarutkan C dengan pembentukan karbida dan Ni 3 C, yang terurai selama kristalisasi lelehan dengan pelepasan grafit; Ni 3 C dalam bentuk bubuk abu-abu-hitam (terurai pada ~ 450 ° C) diperoleh dengan karburasi nikel dalam atmosfer CO pada 250-400 ° C. Nikel terdispersi dengan CO menghasilkan nikel tetrakarbonil Ni(CO) 4 . Ketika menyatu dengan Si, ia membentuk s dan l dan c dan d s; Ni 5 Si 2 , Ni 2 Si dan NiSi melebur secara kongruen resp. pada 1282, 1318 dan 992 °C, Ni 3 Si dan NiSi 2 - secara berurutan. pada 1165 dan 1125 °C, Ni 3 Si 2 terurai tanpa meleleh pada 845 °C. Ketika menyatu dengan B, menghasilkan borida: Ni 3 B (mp. 1175 ° C), Ni 2 B (1240 ° C), Ni 3 B 2 (1163 ° C), Ni 4 B 3 (1580 °С), NiB 12 (2320 °С), NiB (terurai pada 1600 °С). Dengan uap Se, nikel membentuk selenida: NiSe (mp. 980 °C), Ni 3 Se 2 dan NiSe 2 (mereka terurai pada 800 dan 850 °C, masing-masing), Ni 6 Se 5 dan Ni 21 Se 20 (hanya ada di keadaan padat). Ketika nikel menyatu dengan Te, tellurida diperoleh: NiTe dan NiTe 2 (tampaknya, berbagai larutan padat terbentuk di antara mereka), dll.
Arsenat Ni 3 (AsO 4) 2. 8H 2 kristal O-hijau; larutan dalam air 0,022%; to-tami terurai; di atas 200 °С mengalami dehidrasi, pada ~ 1000 °С terurai; katalis sabun padat.
Silika dan t Ni 2 SiO 4 - kristal hijau muda dengan belah ketupat. kisi; padat 4,85 g/cm3 ; terurai tanpa meleleh pada 1545 °C; tidak larut dalam air; buruh tambang. to-tami perlahan terurai saat dipanaskan. Alumina t NiAl 2 O 4 (nikel spinel) - kristal biru dengan kubik. kisi; mp 2110°С; padat 4,50 g/cm3 ; tidak sol. dalam air; perlahan terurai menjadi-tami; katalis hidrogenasi.
Kompleks yang paling penting Comm. nikel-a m m dan n s. Naib. heksaamina dan aquatetramina dengan kation adalah karakteristik, masing-masing. 2+ dan 2+ . Ini adalah kristal biru atau ungu. in-va, biasanya sol. dalam air, dalam larutan warna biru cerah; ketika larutan mendidih dan di bawah aksi to-t terurai; terbentuk dalam larutan selama pemrosesan amonia bijih nikel dan kobalt.
Dalam kompleks Ni(III) dan Ni(IV), koordinasi nomor nikel adalah 6. Contohnya adalah violet K3 dan K2 merah yang dibentuk oleh aksi F2 pada campuran NiCl2 dan KCl; pengoksidasi kuat. Dari jenis lain, garam heteropoliasam diketahui, misalnya. (NH4)6H7. 5H 2 O, sejumlah besar khelat Comm. Ni(II). Lihat juga Senyawa nikel-organik.
Kuitansi. Bijih diproses oleh pyro- dan gidromstal-lurgich. cara. Untuk bijih teroksidasi silikat (tidak dapat menerima pengayaan) gunakan atau pulihkan. peleburan untuk memperoleh feronikel, yang kemudian ditiupkan dalam konverter untuk tujuan pemurnian dan pengayaan, atau peleburan menjadi matte dengan aditif yang mengandung belerang (FeS 2 atau CaSO 4). Matte yang dihasilkan ditiup dalam converter untuk menghilangkan Fe, kemudian digerus dan dibakar, dari NiO yang terbentuk akan direduksi. logam nikel diperoleh dengan cara peleburan. Konsentrat nikel yang diperoleh selama pengayaan bijih sulfida dilebur menjadi matte dengan yang terakhir. bersihkan di konverter. Dari matte tembaga-nikel, setelah pendinginan lambat dengan flotasi, konsentrat Ni 3 S 2 diisolasi, yang, mirip dengan matte dari bijih teroksidasi, dibakar dan direduksi.
Salah satu cara hidroprosesor bijih teroksidasi adalah reduksi bijih dengan gas generator atau campuran H2 dan N2 dengan yang terakhir. pelarutan larutan NH 3 dan CO 2 dengan air purge. Solusinya dimurnikan dari Co dengan amonium sulfida. Selama dekomposisi larutan dengan distilasi NH 3, nikel hidrokso-karbonat mengendap, yang dikalsinasi dan direduksi dari NiO yang terbentuk. mencair mendapatkan Nikel, atau re-solv. dalam larutan NH 3 dan setelah distilasi NH 3 dari pulp dengan reduksi H 2, diperoleh nikel. dr. cara - pencucian bijih teroksidasi dengan asam sulfat dalam autoklaf. Dari larutan yang dihasilkan, setelah pemurnian dan netralisasi, nikel diendapkan dengan hidrogen sulfida di bawah tekanan, dan konsentrat NiS yang dihasilkan diproses seperti matte.
Hidroproses bahan nikel sulfida (konsentrat, mattes) direduksi menjadi pengoksidasi autoklaf. pencucian dengan larutan NH 3 (pada kandungan Co rendah) atau H 2 SO 4 . Dari larutan amonia, setelah pemisahan CuS, nikel diendapkan dengan hidrogen di bawah tekanan. Untuk memisahkan Ni,Co dan Cu dari larutan amonia juga digunakan ekstrak. metode menggunakan, pertama-tama, ekstraktan chelating.
Pencucian oksidasi autoklaf untuk mendapatkan larutan sulfat digunakan baik untuk bahan yang diperkaya (mattes) dengan transfer nikel dan logam lainnya ke larutan, dan untuk konsentrat pyrrhotium Fe 7 S 8 yang buruk. Dalam kasus terakhir, premi teroksidasi. pirhotit, yang memungkinkan untuk mengisolasi unsur S dan konsentrat sulfida, yang selanjutnya dilebur menjadi nikel matte.
Kami menawarkan untuk membeli lembaran nikel NP2 dengan persyaratan yang menguntungkan:
- Banyak pilihan bermacam-macam dan kisaran ukuran.
- Kemungkinan pemrosesan logam tambahan - pemotongan, pembengkokan, galvanisasi, perforasi
- Penjualan potongan dan kosong
- Realisasi produk, baik grosir maupun eceran.
- Harga tanpa komisi perantara.
- Berbagai metode dan syarat pembayaran.
- Sistem diskon yang fleksibel untuk mitra grosir dan reguler.
- Saran profesional gratis.
- Kemungkinan perakitan awal pesanan di gudang.
- Waktu pengiriman cepat. Pengiriman barang berbayar dalam sehari di Moskow.
- Pengiriman ke wilayah Rusia dalam 2-3 hari. Jika perlu, kami akan secara mandiri menghitung dan memesan layanan dari perusahaan transportasi. Pengiriman ke terminal perusahaan transportasi gratis.
- Pengemasan barang sesuai dengan kebutuhan pelanggan. Dimungkinkan untuk menggunakan beberapa jenis kemasan: lingkaran poliester PET dan film polietilen PVC.
- Kemampuan untuk menyimpan barang di gudang kami sampai pengiriman.
- Pengembalian barang sesuai dengan undang-undang Federasi Rusia.
Karakteristik dan ukuran bermacam-macam.
Lembaran nikel NP2 adalah produk setengah jadi persegi panjang datar yang diproduksi dengan rolling panas.
Keuntungan dari lembaran nikel meliputi:
- kekuatan tinggi;
- ketahanan terhadap kerusakan korosi;
- ketahanan terhadap suhu ekstrem;
- sifat magnet (ferromagnet).
Karakteristik produk ditentukan oleh sifat-sifat kadar nikel NP2 - yang disebut. nikel setengah jadi menurut GOST 492-2006. Standar mengatur kandungan pengotor (karbon, tembaga, besi, magnesium, dll.) dalam logam - total tidak lebih dari 0,5% berat. Bahan tersebut memiliki ketahanan panas (ketahanan terhadap tekanan mekanis pada suhu tinggi), ketahanan terhadap kerusakan korosi di banyak lingkungan agresif, termasuk pada suhu tinggi (sifat ini didefinisikan sebagai ketahanan panas).
Ketebalan lembaran menurut GOST bervariasi dari 5 hingga 20 mm, lebar - 500, 600, 700, 800 mm, panjang 500-2000 mm. Anda dapat membeli lembaran nikel yang diukur panjangnya, kelipatan 100 mm, dan acak, sepenuhnya sesuai dengan standar negara.
Kualitas produk dikendalikan pada semua tahap proses produksi. Permukaan material memenuhi standar dan tidak memiliki delaminasi, kerusakan mekanis dan cacat lainnya.
GOST, TU, dan standar lainnya.
Lembar spesifikasi NP2 ditentukan oleh GOST 6235-91. Presisi tinggi pembuatan dan penyelesaian produk diatur oleh GOST 26877-2008. Komposisi kimia nikel NP2 sesuai dengan GOST 492-2006.
Area aplikasi.
Sifat mekanik, listrik, anti korosi yang baik, menyebabkan meluasnya penggunaan lembaran NP2. Secara khusus, penggunaannya dibenarkan dalam produksi, di mana tuntutan tinggi ditempatkan pada ketahanan korosi material. Arahan utama penggunaan:
- pembuatan kapal;
- teknik mesin, pembuatan instrumen;
- bagian listrik - katoda, anoda;
- produksi produk untuk industri kimia - wadah, ketel, piring yang berinteraksi dengan zat agresif.
Penjualan lembaran nikel dari gudang di Moskow.
Penjualan lembaran nikel dilakukan dari gudang di Moskow, yang terletak di:
111123, Moskow, sh. Enthusiastov, 56, gedung 44
Anda dapat menerima barang berbayar dengan pengiriman sendiri atau pengiriman, yang akan dilakukan oleh perusahaan kami. Armada kendaraan kami sendiri, yang terdiri dari mobil dengan berbagai tonase, akan memungkinkan kami untuk mengirimkan pesanan ke objek Anda dengan murah dan cepat.
Saat memesan produk dari 100 kg. pengiriman akan gratis untuk Anda.
Pengiriman dan pengiriman barang yang dibayar dilakukan dalam satu hari.
Nikel sulfat adalah zat kristal berwarna hijau zamrud atau pirus, larut dalam air, lapuk di udara. Ini adalah salah satu jenis garam nikel.
Nikel sulfat adalah zat yang sangat beracun, jadi ketika bekerja dengannya, Anda harus mengikuti aturan untuk menangani zat berbahaya.
Rumus kimia: NiSO4 7H2O.
Nikel sulfat digunakan dalam elektroplating untuk pelapisan nikel produk dan logam.
Dan juga - untuk pembuatan baterai, katalis, ferit dalam industri elektronik dan listrik, dalam metalurgi untuk persiapan paduan. Nikel telah menemukan aplikasi luas dalam industri parfum, lemak dan kimia sebagai reagen.
Dalam produksi keramik, nikel sulfat digunakan sebagai pewarna.
Persyaratan keamanan untuk nikel sulfat (nikel sulfat heptahidrat, nikel vitriol) GOST 4465-74.
Nikel sulfat 7-air (II) adalah zat kristal. Ketika tertelan, ia memiliki efek karsinogenik dan toksik umum. Jika terjadi kontak dengan kulit dan selaput lendir saluran pernapasan bagian atas dan mata, produk ini mengiritasi dan menyebabkan hipersensitivitas terhadap nikel.
Saat melarutkan nikel sulfat 7-air (II) dalam air, hidroaerosol terbentuk, yang, menurut tingkat dampak pada tubuh, termasuk dalam zat kelas bahaya 1.
Konsentrasi maksimum hidroaerosol nikel sulfat 7-air dalam hal nikel di udara wilayah kerja yang diizinkan adalah 0,005 mg/m³.
Konsentrasi maksimum ion nikel yang diperbolehkan dalam air waduk untuk penggunaan sanitasi adalah 0,1 mg/dm³.
Netralisasi dan penghancuran nikel sulfat 7-air tidak dikenakan. Produk yang tumpah setelah pembersihan kering dan basah selanjutnya dibuang dalam proses teknologi untuk produksi atau konsumsi nikel sulfat.
Nikel sulfat tidak membentuk zat beracun di udara dan limbah.
Nikel sulfat 7-air (II) tidak mudah terbakar, tahan api dan ledakan.
Semua orang yang bekerja dengan nikel sulfat harus dilengkapi dengan pakaian khusus, alas kaki khusus dan peralatan pelindung lainnya. Untuk melindungi sistem pernapasan, respirator ShB-1 "Petal" harus digunakan. Untuk menghindari kontak dengan kulit tangan, disarankan untuk menggunakan pasta pelindung IER-2 dan salep lanolin-castor. Jika nikel sulfat masuk ke mata, bilas dengan banyak air.
Tempat produksi dan laboratorium di mana pekerjaan dengan nikel sulfat 7-air dilakukan harus dilengkapi dengan ventilasi suplai dan pembuangan, peralatan harus disegel.
DEFINISI
Nikel adalah elemen kedua puluh delapan dari Tabel Periodik. Penunjukan - Ni dari bahasa Latin "niccolum". Berada di periode keempat, kelompok VIIIB. Mengacu pada logam. Muatan inti adalah 28.
Seperti kobalt, nikel terdapat di alam terutama dalam bentuk senyawa dengan arsenik atau belerang; seperti, misalnya, adalah mineral kupfernikel NiAs, kilau arsenik-nikel NiAsS, dll. Nikel lebih umum daripada kobalt [sekitar 0,01% (massa) kerak bumi].
Nikel logam memiliki warna keperakan dengan warna kekuningan (Gbr. 1), sangat keras, dipoles dengan baik, dan ditarik oleh magnet. Hal ini ditandai dengan ketahanan korosi yang tinggi - stabil di atmosfer, dalam air, dalam alkali dan sejumlah asam. Ini secara aktif larut dalam asam nitrat. Ketahanan kimia nikel adalah karena kecenderungannya untuk pasif - pada pembentukan film oksida di permukaan, yang memiliki efek perlindungan yang kuat.
Beras. 1. Nikel. Penampilan.
Berat atom dan molekul nikel
DEFINISI
Berat molekul relatif suatu zat (M r) adalah angka yang menunjukkan berapa kali massa molekul tertentu lebih besar dari 1/12 massa atom karbon, dan massa atom relatif suatu unsur (A r)- berapa kali massa rata-rata atom suatu unsur kimia lebih besar dari 1/12 massa atom karbon.
Karena nikel ada dalam keadaan bebas dalam bentuk molekul Ni monoatomik, nilai massa atom dan molekulnya bertepatan. Mereka sama dengan 58,6934.
Isotop nikel
Diketahui bahwa nikel dapat terdapat di alam dalam bentuk lima isotop stabil yaitu 58Ni, 60Ni, 61Ni, 62Ni, dan 64Ni. Nomor massa mereka masing-masing adalah 58, 60, 61, 62 dan 64. Inti isotop nikel 58 Ni mengandung dua puluh delapan proton dan tiga puluh neutron, dan isotop yang tersisa hanya berbeda dalam jumlah neutron.
Ada isotop nikel tidak stabil buatan dengan nomor massa dari 48 hingga 78, serta delapan keadaan metastabil, di antaranya isotop 59 Ni dengan waktu paruh 76 ribu tahun adalah yang berumur paling panjang.
ion nikel
Rumus elektronik yang menunjukkan distribusi orbital elektron nikel adalah sebagai berikut:
1s 2 2s 2 2p 6 3s 2 3p 6 3d 8 4s 2 .
Sebagai hasil interaksi kimia, nikel melepaskan elektron valensinya, yaitu adalah donor mereka, dan berubah menjadi ion bermuatan positif:
Ni 0 -2e → Ni 2+;
Ni 0 -3e → Ni 3+.
Molekul dan atom nikel
Dalam keadaan bebas, nikel ada dalam bentuk molekul Ni monoatomik. Berikut adalah beberapa sifat yang mencirikan atom dan molekul nikel:
Paduan nikel
Sebagian besar nikel digunakan untuk memproduksi berbagai paduan dengan besi, tembaga, seng, dan logam lainnya. Penambahan nikel pada baja meningkatkan ketangguhan dan ketahanannya terhadap korosi.
Paduan berbasis nikel dapat dibagi menjadi tahan panas (nimonic, inconel, hastella [lebih dari 60% nikel, 15-20% kromium dan logam lainnya]), magnetik (permalloy) dan paduan dengan sifat khusus (logam monel, nikelin, konstantan , invar, platina).
Contoh pemecahan masalah
CONTOH 1
| Tugas | Tuliskan persamaan reaksi yang dapat digunakan untuk melakukan transformasi berikut: NiCl 2 → Ni → NiSO 4 → Ni(NO 3) 2 → Ni(OH) 2 → NiCl 2. Gambarkan persamaan reaksi yang terjadi dalam larutan dalam bentuk ionik dan disingkat ion. |
| Menjawab | Dengan menempatkan larutan nikel (II) klorida yang lebih aktif daripada logam nikel, dimungkinkan untuk memperoleh nikel dalam bentuk bebasnya (reaksi substitusi): NiCl 2 + Zn → Ni + ZnCl 2 ; Ni 2+ + Zn 0 → Ni 0 + Zn 2+ . Nikel dilarutkan dalam asam sulfat encer untuk membentuk nikel(II) sulfat: Ni + H 2 SO 4 (encer) → NiSO 4 + H 2; Ni 0 + 2H + → Ni 2+ + H 2 . Nikel (II) nitrat dapat diperoleh dengan reaksi pertukaran: NiSO 4 + Ba(NO 3) 2 → Ni(NO 3) 2 + BaSO 4 ; SO 4 2- + Ba 2+ → BaSO 4 . Dengan bekerja pada nikel (II) nitrat dengan alkali, nikel (II) hidroksida dapat diperoleh: Ni(NO 3) 2 + 2NaOH → Ni(OH) 2 + 2NaNO 3 ; Ni 2+ + 2OH - \u003d Ni (OH) 2 . Nikel(II) klorida dari nikel(II) hidroksida dapat diperoleh dengan reaksi netralisasi dengan asam klorida: Ni(OH) 2 + 2HCl → NiCl 2 + 2H 2 O; OH - + H + \u003d H 2 O. |
CONTOH 2
| Tugas | Berapa massa nikel (II) klorida yang dapat diperoleh dengan memanaskan 17,7 g nikel dan 12 liter klorin (n.o.)? Berapa volume larutan 0,06 M yang dapat dibuat dari massa garam ini? |
| Larutan | Mari kita tulis persamaan reaksinya: Ni + Cl 2 \u003d NiCl 2. Mari kita cari jumlah mol nikel (massa molar - 59 g / mol) dan klorin yang telah bereaksi menggunakan data yang ditunjukkan dalam kondisi masalah: n (Ni) = m (Ni) / M (Ni); n (Ni) \u003d 17,7 / 59 \u003d 0,3 mol. n (Cl 2) \u003d V (Cl 2) / V m; n (Cl 2) \u003d 12 / 22,4 \u003d 0,54 mol. Berdasarkan persamaan soal n (Ni): n (Cl 2) = 1:1. Ini berarti klorin berlebih dan semua perhitungan lebih lanjut harus dilakukan dengan menggunakan nikel. Mari kita cari jumlah zat dan massa nikel (II) klorida yang dihasilkan (massa molar 130 g / mol): n (Ni): n (NiCl 2) = 1:1; n (Ni) \u003d n (NiCl 2) \u003d 0,3 mol. m (NiCl 2)= n (NiCl 2)×M (NiCl 2); m (NiCl 2) \u003d 0,3 × 130 \u003d 39 g. Hitung volume larutan 0,06M yang dapat diperoleh dari 39 g nikel (II) klorida: V (NiCl 2) \u003d n (NiCl 2) / c (NiCl 2); V (NiCl 2) \u003d 0,3 / 0,06 \u003d 0,5 l. |
| Menjawab | Massa nikel (II) klorida adalah 39 g, volume larutan 0,06M adalah 0,5 l (500 ml). |
Bagian 1. Karakteristik.
Bagian 2. Berada di alam.
Bagian 3. Tanda Terima.
Bagian 4. Aplikasi.
- Ayat 1. Paduan.
- Ayat 2. Pelapisan nikel.
Bagian 5. Koin.
Ni- ini adalah elemen dari subkelompok samping dari kelompok kedelapan, periode keempat dari sistem periodik unsur kimia D. I. Mendeleev, dengan nomor atom 28.
Karakteristik nikel
Ni- berwarna putih keperakan, tidak luntur di udara. Ini memiliki kisi kubik berpusat pada wajah dengan Titik a = 0,35238 HM, grup ruang Fm3m. Dalam bentuknya yang murni, dapat diproses dengan tekanan. Ini adalah feromagnet dengan titik Curie 358 C.
Hambatan listrik spesifik 0,0684 Ohm∙m.
Koefisien ekspansi termal linier =13.5∙10-6 K-1 pada 0 C
Koefisien ekspansi termal volumetrik =38—39∙10-6 K-1
Modulus elastisitas 196-210 GPa.
Atom nikel memiliki konfigurasi elektron eksternal 3d84s2. Tingkat oksidasi nikel yang paling stabil adalah nikel(II).
Ni membentuk senyawa dengan bilangan oksidasi +2 dan +3. Pada saat yang sama, Ni dengan bilangan oksidasi +3 hanya dalam bentuk garam kompleks. Untuk senyawa nikel +2, sejumlah besar senyawa biasa dan kompleks diketahui. Nikel oksida Ni2O3 adalah oksidator kuat.

Ni dicirikan oleh ketahanan korosi yang tinggi - stabil di udara, dalam air, dalam alkali, dan dalam sejumlah asam. Resistensi kimia disebabkan oleh kecenderungannya untuk pasif - pembentukan film oksida padat pada permukaannya, yang memiliki efek perlindungan. Ni aktif larut dalam asam nitrat.
Dengan karbon monoksida CO Ni dengan mudah membentuk nikel karbonit (CO)4 yang mudah menguap dan sangat beracun.
Serbuk nikel yang terdispersi halus bersifat piroforik (menyala sendiri di udara).
Ni terbakar hanya dalam bentuk bubuk. Ini membentuk dua nikelO dan Ni2O3 oksida dan, masing-masing, dua nikel(OH)2 dan nikel(OH)3 hidroksida. Garam nikel terlarut yang paling penting adalah asetat, klorida, nitrat, dan sulfat.


Larutan biasanya berwarna hijau, sedangkan garam anhidrat berwarna kuning atau coklat-kuning. Garam yang tidak larut termasuk oksalat dan fosfat (hijau), tiga sulfida:
nikelS (hitam)
Ni3S2 (perunggu kekuningan)
Ni3S4 (putih perak).
Ni juga membentuk banyak koordinasi dan senyawa kompleks.
Larutan berair dari garam nikel(II) mengandung ion heksaaquanikel(II) nikel(H2O)62+. Ketika larutan amonia ditambahkan ke larutan yang mengandung ion-ion ini, nikel (II) hidroksida, zat agar-agar hijau, mengendap. Endapan ini larut ketika jumlah amonia yang berlebihan ditambahkan karena pembentukan ion heksaminnikel (II) nikel(NH3)62+.
Ni membentuk kompleks dengan struktur persegi tetrahedral dan planar. Misalnya, kompleks tetrakloronikkelat (II) NiCl42– memiliki struktur tetrahedral, sedangkan kompleks nikel(CN)42– tetrasianonikkelat (II) memiliki struktur persegi planar.
Analisis kualitatif dan kuantitatif menggunakan larutan alkali butanedionedioxime, juga dikenal sebagai dimethylglyoxime, untuk mendeteksi ion nikel(II). Ketika berinteraksi dengan ion nikel (II), senyawa koordinasi merah bis (butanedionedioxymato) Ni (II) terbentuk. Ini adalah khelat dan ligan butanedionedioksimato adalah bidentat.
Ni alam terdiri dari 5 isotop stabil, 58 nikel, 60 nikel, 61 nikel, 62 nikel yang paling melimpah (68,077% kelimpahan alami).
Berada di alam
Ni cukup umum di alam - kandungannya di kerak bumi sekitar 0,01% (berat). Itu terjadi di kerak bumi hanya dalam bentuk terikat; meteorit besi mengandung Ni asli (hingga 8%). Kandungannya dalam batuan ultrabasa kira-kira 200 kali lebih tinggi daripada di batuan asam (1,2 kg/t dan 8 g/t). Pada batuan ultrabasa, jumlah nikel yang dominan berasosiasi dengan olivin yang mengandung 0,13-0,41% nikel. Ini juga menggantikan magnesium secara isomorfik.
Sebagian kecil nikel hadir dalam bentuk sulfida. Ni menunjukkan sifat siderofilik dan kalkofilik. Dengan peningkatan kandungan belerang dalam magma, nikel sulfida muncul bersama dengan tembaga, kobalt, besi dan platinoid. Dalam proses hidrotermal, bersama dengan kobalt, arsenik dan Abu-abu dan kadang-kadang dengan bismut, uranium, dan perak, Ni membentuk konsentrasi tinggi sebagai arsenida nikel dan sulfida. Ni umumnya ditemukan dalam bijih tembaga-nikel yang mengandung sulfida dan arsenik.
Nikel (pirit nikel merah, kupfernikel) nikel As.

Kloantit (nikel pirit putih) (nikel, Co, Fe)As2
Garnierit (Mg, nikel)6(Si4O11)(OH)6 dengan H2O dan silikat lainnya.

Pirit magnetik (Fe, nikel, Cu)S
Kilau arsenik-nikel (gersdorfite) nikel As S,
Pentlandit (Fe, Nikel) 9S8
Banyak yang diketahui tentang nikel dalam organisme. Telah ditetapkan, misalnya, bahwa kandungannya dalam darah manusia berubah seiring bertambahnya usia, bahwa pada hewan jumlah nikel dalam tubuh meningkat, dan akhirnya, ada beberapa tanaman dan mikroorganisme - "konsentrator" nikel, yang mengandung ribuan dan bahkan ratusan ribu kali lebih banyak nikel daripada Lingkungan.
Kuitansi
Total cadangan bijih nikel pada awal tahun 1998 diperkirakan mencapai 135 juta ton, termasuk yang dapat diandalkan - 49 juta ton Bijih nikel utama adalah nikel (kupfernickel) nikel As, nikel millerit S, pentlandit (Fe nikel)9S8 - juga mengandung arsenik, besi Dan sulfur; Inklusi pentlandit juga terjadi pada pirhotit beku. Bijih lain dari mana nikel juga ditambang mengandung pengotor Co, Cu, Fe dan Mg. Terkadang Ni adalah komoditas utama proses pemurnian, tetapi lebih sering diperoleh sebagai produk sampingan produk dalam teknologi logam lainnya. Dari cadangan yang dapat diandalkan, menurut berbagai sumber, dari 40 hingga 66% nikel berada dalam bijih nikel teroksidasi (ONR),
33% dalam sulfida. Sampai tahun 1997, pangsa nikel yang dihasilkan dari pengolahan OHP adalah sekitar 40% dari produksi dunia. Dalam kondisi industri, OHP dibagi menjadi dua jenis: magnesian dan besi.
Bijih magnesian tahan api, sebagai suatu peraturan, mengalami peleburan listrik untuk feronikel (5-50% nikel + Co, tergantung pada komposisi bahan baku dan fitur teknologi).
Bijih laterit yang paling mengandung besi diproses dengan metode hidrometalurgi menggunakan pencucian amonia-karbonat atau pencucian autoklaf asam sulfat. Tergantung pada komposisi bahan baku dan skema teknologi yang diterapkan, produk akhir dari teknologi ini adalah: nikel oksida (76-90% nikel), sinter (89% nikel), konsentrat sulfida dari berbagai komposisi, serta logam Ni. elektrolit, bubuk nikel dan kobalt.
Kurang mengandung besi - bijih nontronite dilebur menjadi matte. Di perusahaan yang beroperasi pada siklus penuh, skema pemrosesan lebih lanjut mencakup konversi, pemanggangan matte, peleburan listrik oksida nikel untuk mendapatkan nikel logam. Dalam perjalanannya, kobalt yang diekstraksi diproduksi dalam bentuk logam dan/atau garam. Sumber nikel lain: di abu batubara South Wales di Inggris - hingga 78 kg nikel per ton. Peningkatan kandungan nikel dalam beberapa batubara, minyak, serpih menunjukkan kemungkinan konsentrasi nikel oleh bahan organik fosil. Alasan untuk fenomena ini belum dijelaskan.
“Ni tidak dapat diperoleh dalam waktu lama dalam bentuk plastis karena selalu memiliki sedikit campuran belerang dalam bentuk nikel sulfida, terletak di lapisan tipis dan rapuh di perbatasan. logam. Penambahan sejumlah kecil magnesium ke dalam nikel cair mengubah belerang menjadi bentuk senyawa dengan magnesium, yang mengendap dalam bentuk butiran tanpa melanggar plastisitas. logam».
Sebagian besar nikel diperoleh dari garnierit dan pirit magnetik.

Bijih silikat direduksi dengan debu batubara dalam tungku tabung putar menjadi pelet besi-nikel (5-8% nikel), yang kemudian dimurnikan dari belerang, dikalsinasi dan diolah dengan larutan amonia. Setelah larutan diasamkan, logam diperoleh secara elektrolitik darinya.
Metode karbonil (metode Mond). Pertama, matte tembaga-nikel diperoleh dari bijih sulfida, di mana kobalt dilewatkan di bawah tekanan tinggi. Nikel nikel(CO)4 tetrakarbonil yang mudah menguap terbentuk, dan terutama logam murni diisolasi dengan dekomposisi termal.
Metode aluminotermik pemulihan nikel dari bijih oksida: 3NiO + 2Al = 3Ni + Al2O.
Aplikasi
Paduan
Ni adalah dasar dari sebagian besar superalloy, bahan bersuhu tinggi yang digunakan dalam industri dirgantara untuk suku cadang pembangkit listrik.
logam monel (65 - 67% nikel + 30 - 32% Cu+ 1% Mn), tahan panas hingga 500 °C, sangat tahan korosi;
putih (585 mengandung 58,5% emas dan paduan (ligatur) perak dan nikel (atau paladium));

Nichrome, paduan resistensi (60% Nikel + 40% Cr);
Permalloy (76% nikel + 17% Fe + 5% Cu + 2% Cr), memiliki kerentanan magnet yang tinggi dengan kerugian histeresis yang sangat rendah;

Invar (65% Fe + 35% Nikel), hampir tidak memanjang saat dipanaskan;

Selain itu, paduan nikel termasuk baja nikel dan kromium-nikel, perak nikel, dan berbagai paduan resistansi seperti konstantan, nikel, dan manganin.
Pipa nikel digunakan untuk pembuatan kapasitor dalam produksi hidrogen, untuk memompa alkali dalam industri kimia. Alat tahan bahan kimia nikel banyak digunakan dalam bidang kedokteran dan penelitian. Ni digunakan untuk radar, televisi, remote control proses dalam teknologi nuklir.
Nikel murni digunakan untuk membuat peralatan kimia, berbagai peralatan, perangkat, boiler dengan ketahanan korosi yang tinggi dan sifat fisik yang konstan, dan dari bahan nikel - reservoir dan tangki untuk menyimpan produk makanan, bahan kimia, minyak esensial, untuk mengangkut alkali, untuk melelehkan kaustik alkali.
Atas dasar bubuk nikel murni, filter berpori dibuat untuk menyaring gas, bahan bakar, dan produk lainnya dalam industri kimia. industri. Bubuk Ni juga dikonsumsi dalam produksi paduan nikel dan sebagai pengikat dalam pembuatan bahan keras dan superhard.
Peran biologis nikel mengacu pada jumlah elemen yang diperlukan untuk perkembangan normal organisme hidup. Namun, sedikit yang diketahui tentang perannya dalam organisme hidup. Ni diketahui berperan dalam reaksi enzimatik pada hewan dan tumbuhan. Pada hewan, itu terakumulasi di jaringan keratin, terutama di bulu. Peningkatan kandungan nikel dalam tanah menyebabkan penyakit endemik - bentuk jelek muncul pada tanaman, dan penyakit mata pada hewan terkait dengan akumulasi nikel di kornea. Dosis toksik (untuk tikus) - 50 mg. Yang sangat berbahaya adalah senyawa nikel yang mudah menguap, khususnya, nikel tetrakarbonil (CO)4-nya. MPC senyawa nikel di udara berkisar antara 0,0002 hingga 0,001 mg/m3 (untuk berbagai senyawa).
Ni adalah penyebab utama alergi (dermatitis kontak) terhadap logam yang bersentuhan dengan kulit (perhiasan, jam tangan, kancing denim).
Di Uni Eropa, kandungan nikel dalam produk yang bersentuhan dengan kulit manusia terbatas.
Nikel karbonit Nikel(CO) sangat beracun. Konsentrasi maksimum yang diizinkan dari uapnya di udara tempat industri adalah 0,0005 mg/m3.
Pada abad ke-20, ditemukan bahwa pankreas sangat kaya akan nikel. Ketika diberikan setelah insulin, nikel memperpanjang kerja insulin dan dengan demikian meningkatkan aktivitas hipoglikemik. Ni mempengaruhi proses enzimatik, oksidasi asam askorbat, mempercepat transisi gugus sulfhidril menjadi disulfida. Ni dapat menghambat aksi adrenalin dan menurunkan tekanan darah. Kelebihan asupan nikel dalam tubuh menyebabkan vitiligo. Ni disimpan di pankreas dan kelenjar paratiroid.
pelapisan nikel
Pelapisan nikel adalah pembuatan lapisan nikel pada permukaan logam lain untuk melindunginya dari korosi. Ini dilakukan dengan cara galvanik menggunakan elektrolit yang mengandung nikel(II) sulfat, natrium klorida, boron hidroksida, surfaktan dan zat mengkilap, dan anoda nikel terlarut. Ketebalan lapisan nikel yang dihasilkan adalah 12–36 m. Stabilitas kilap permukaan dapat dipastikan dengan pelapisan krom berikutnya (ketebalan lapisan kromium 0,3 m).
Pelapisan nikel tanpa arus dilakukan dalam larutan campuran nikel(II) klorida dan campuran natrium hipofosfit dengan adanya natrium sitrat:
NiCl2 + NaH2PO2 + H2O = Nikel + NaH2PO3 + 2HCl
proses dilakukan pada pH 4 – 6 dan 95 °C
Yang paling umum adalah pelapisan nikel elektrolitik dan kimia. Lebih sering pelapisan nikel (disebut matte) diproduksi dengan metode elektrolitik. Yang paling banyak dipelajari dan stabil di kerja elektrolit sulfat. Ketika ditambahkan ke elektrolit, kilau pembentuk dilakukan oleh apa yang disebut pelapisan nikel cerah. Pelapis elektrolit memiliki beberapa porositas, yang tergantung pada ketelitian persiapan permukaan substrat dan pada ketebalan lapisan. Untuk melindungi dari korosi, tidak adanya pori-pori sama sekali diperlukan, oleh karena itu, lapisan multilayer diterapkan, yang, dengan ketebalan yang sama, lebih dapat diandalkan daripada lapisan tunggal (misalnya, baja barang dagangan sering dilapisi sesuai dengan skema Cu - Nikel - Cr).

Kerugian dari pelapisan nikel elektrolitik adalah pengendapan nikel yang tidak merata pada permukaan relief dan ketidakmungkinan melapisi lubang yang sempit dan dalam, rongga, dll. Pelapisan nikel kimia agak lebih mahal daripada pelapisan nikel elektrolitik, tetapi memberikan kemungkinan penerapan lapisan dengan ketebalan dan kualitas yang seragam pada setiap bagian permukaan relief, asalkan tersedia solusi untuk mereka. Proses ini didasarkan pada reaksi reduksi ion nikel dari garamnya menggunakan campuran hipofosfit natrium (atau zat pereduksi lainnya) dalam larutan berair.
Pelapisan nikel digunakan, misalnya, untuk melapisi bagian peralatan kimia, mobil, sepeda, peralatan medis, perangkat.
Ni juga digunakan untuk melilitkan alat musik senar.

mata uang
Ni banyak digunakan dalam produksi koin di banyak negara. Di Amerika Serikat, koin 5 sen bahasa sehari-hari disebut "Ni".
Ni telah menjadi komponen koin sejak pertengahan abad ke-19. Di Amerika Serikat, istilah "Ni" atau "Nick" awalnya digunakan untuk koin tembaga-nikel (elang terbang), yang menggantikan tembaga dengan 12% nikel pada tahun 1857-58.

Masih kemudian pada tahun 1865, istilah yang diberikan untuk tiga persen nikel meningkat sebesar 25%. Pada tahun 1866 lima persen nikel (25% nikel, 75% tembaga). Seiring dengan paduan proporsi, istilah itu saat ini digunakan di Amerika Serikat. Koin nikel hampir murni pertama kali digunakan pada tahun 1881 di Swiss, dan khususnya, lebih dari 99,9% Ni dari koin lima sen dicetak di Kanada (produsen nikel terbesar di dunia pada saat itu).
sen yang terbuat dari nikel" height="431" src="/pictures/investments/img778307_14_Britanskie_monetyi_v_5_i_10_penny_sdelannyie_iz_nikelya.jpg" title="(!LANG:14. Koin 5 dan 10 sen Inggris yang terbuat dari nikel" width="682" />!}
Italia 1909" height="336" src="/pictures/investments/img778308_15_Monetyi_iz_nikelya_Italiya_1909_god.jpg" title="(!LANG:15. Koin nikel, Italia 1909" width="674" />!}
Sumber
Wikipedia - Ensiklopedia Gratis, WikiPedia
hyperon-perm.ru - Produksi Hyperon
cniga.com.ua - Portal Buku
chem100.ru - Buku Pegangan Ahli Kimia
bse.sci-lib.com - Arti kata-kata dalam Ensiklopedia Besar Soviet
chemistry.narod.ru - Dunia Kimia
dic.academic.ru - Kamus dan ensiklopedia
Ensiklopedia investor. 2013 .
Sinonim:- Nikaragua
Lihat apa itu "Nikel" di kamus lain:
NIKEL- (simbol Ni), logam dengan berat atom 58,69, nomor seri 28, termasuk kobalt dan besi dalam golongan VIII dan baris ke-4 sistem periodik Mendeleev. Oud. di dalam. 8.8, titik leleh 1452°. Dalam hubungan mereka yang biasa, N. ... ... Ensiklopedia Medis Besar
NIKEL- (simbol Ni), logam putih keperakan, ELEMEN TRANSISI, ditemukan pada tahun 1751. Bijih utamanya: bijih nikel-besi sulfida (pentlandit) dan nikel arsenida (nikel). Nikel memiliki proses pemurnian yang kompleks, termasuk dekomposisi yang berbeda ... ... Kamus ensiklopedis ilmiah dan teknis
NIKEL- (Nikel Jerman). Logam ini berwarna putih keperakan dan tidak ditemukan dalam bentuk murni. Baru-baru ini, telah digunakan untuk mengganti peralatan makan dan peralatan dapur. Kamus kata-kata asing termasuk dalam bahasa Rusia. Chudinov A.N., 1910. NIKEL Jerman. Nikel… Kamus kata-kata asing dari bahasa Rusia
Nikel- adalah logam putih keabu-abuan yang relatif keras dengan titik leleh 1453 derajat. C. Bersifat feromagnetik, mudah dibentuk, ulet, kuat, dan tahan terhadap korosi dan oksidasi. Nikel sebagian besar ... ... Terminologi resmi
nikel- saya, m. nikel m. , Jerman Nikel. 1. Logam tahan api berwarna putih keperakan. BAS 1. Nikel, pendamping bijih perak yang berbahaya, mendapatkan namanya dari nama kurcaci jahat yang diduga tinggal di tambang Saxon. Fersman Zanim. geokimia. 2. Lapisan atas ... ... Kamus Sejarah Gallicisms of the Russian Language
NIKEL- (lat. Niccolum) Ni, unsur kimia golongan VIII dari sistem periodik, nomor atom 28, massa atom 58,69. Nama tersebut berasal dari German Nickel, nama roh jahat yang diduga mengganggu para penambang. logam putih keperakan; kepadatan 8,90 g/cm³, mp 1455… … Kamus Ensiklopedis Besar
NIKEL- NIKEL, nikel, suami. (Nikel Jerman). Logam tahan api putih keperakan, upr. untuk pembuatan perkakas, perkakas, dll. (Setelah nama dewa gunung dalam mitologi Skandinavia.) Kamus Penjelasan Ushakov. D.N. Ushakov. 1935 1940 ... Kamus Penjelasan Ushakov